元素周期表错了?Nature新论文引发争议
铹——这种由化学家创造的、本不存在于自然界的元素,到底属于元素周期表的哪个位置?这一直是学界争论的焦点,而最近,一项新的实验结果又将这一争论推上风口浪尖。
撰文 戴维·卡斯特维奇(Davide Castelvecchi)
翻译 丁家琦
审校 吴兰
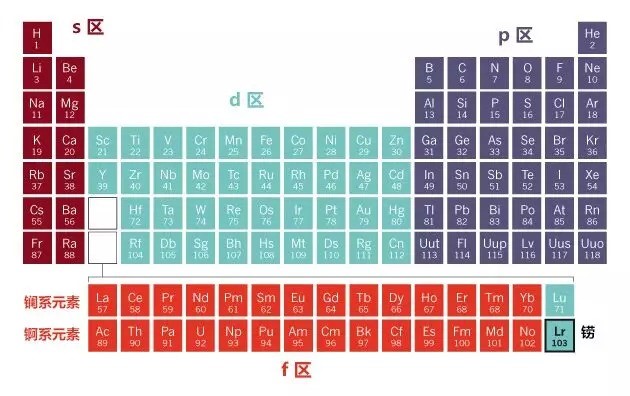
铹是第103号元素,位于元素周期表中f区的末尾。
物理学家对人工放射性元素铹(lawrencium)——位于元素周期表中f区末尾的第103号元素——进行了最新测量,而测量的结果可能会点燃一场奇妙的争论:这个元素到底应该处在周期表上的哪个位置?更有意思的是,争论的战火甚至会蔓延到周期表本身的结构是否合理上。
在2015年4月9日的Nature上,一个由物理学家与化学家组成的国际研究团队发表论文(Measurement of the first ionization potential of lawrencium, element 103,http://www.nature.com/nature/journal/v520/n7546/full/nature14342.html), 他们测量了铹原子失去最外层的一个电子而变成离子所需要的能量——即“第一电离能”。测试结果出乎研究者的意料:这个能量非常之小。铹元素是一种放射性元 素,自然中并不存在,人工合成也只能得到一点点,并且几秒钟之后就会消失,所以,科学家对其完成的这次测量堪称化学领域的杰作。
铹元素的英文写做lawrencium,以发明回旋加速器的物理学家Ernest Lawrence命名。迄今为止,在我们能够测量到第一电离能(first ionization energy)的元素中,铹元素是最重的一个。测量第一电离能有助于研究者了解原子的化学性质,但在此之前,科学家最多只能测量到99号元素锿 (einsteinium)的第一电离能。
超重原子
为了制造铹元素,日本东海的日本原子能机构(JAEA)的研究者将硼(boron)原子打到一个用锎(californium)原子制成的“靶”上(锎本身也是人工同位素),每几秒钟就可以制造出一个铹-256原子,它有103个质子和153个中子,半衰期约为27秒。
研究人员用碘化镉的喷雾捕捉到了这些原子,并将其沉积在加热到2 700开尔文的金属表面上。这么高的温度足以将一些铹原子最外层的一个电子“脱下”,而只要数出有多少个原子按这种方式发生电离,就能得到铹原子电离一个 电子所需的能量(即第一电离能)。JAEA的化学家Tetsuya Sato说,这个能量出乎意料地低,仅为4.96电子伏特,这在整个元素周期表中排倒数第5。
实验显示,铹的最外层电子被束缚得很“松”,跟周期表最左一栏的元素(如钠和钾)类似,这也与文章的共同作者、以色列特拉维夫大学(Tel Aviv University)研究者的理论预测相符合。这意味着,铹元素到底该处于周期表的什么位置,似乎又要引起一番争论。
锕系元素之争
为了描述元素的最外层电子排布,周期表被划为不同的栏与分区。根据元素电子轨道的不同类型,元素被分在s区、p区、d区和f区。所谓电子轨道,是指围绕着原 子核的电子最有可能占据的一片“云”一样的空间区域。区域的性状可以通过量子力学计算出来:s轨道呈圆形,p轨道成哑铃状,其他轨道就更复杂了。元素失去 与得到最外层电子的难易,标志着该元素发生化学反应的活性——这就是为什么周期表中同一竖栏的元素的化学性质往往类似的原因。
有些化学家 认为,铹元素(以及位于它正上方的“亲戚”镥,lutetium,简写为Lu)的化学性质与周期表d区最左侧的钪(Sc)和钇(Y)相似,因此应该把它放 在钪和钇的下面,归d区。但是,大多数标准的周期表并没有这么做:它们将铹放在镧系和锕系两列元素的最后。镧系和锕系共包含两行、共30个元素,大多数周 期表将这两行元素作为附件,放在整个表的底部。而其他的一些周期表,包括化学界最权威的学会——国际纯粹与应用化学联合会(IUPAC)官方提供的周期 表,则认为整个f区(即镧系和锕系元素)都应当隶属于钪和钇下方的两个位置,完全是d区的一部分。
不管d区和f区之争如何,实验和数值模 拟都显示,铹原子的最外层电子占据的是哑铃形的p轨道。课本上可能会讲“这一元素的p轨道未被占据”,但因为铹的内层电子运动速度很快(接近光速!),狭 义相对论产生的层叠效应使该p轨道能量降低。在其他的超重元素,例如钅喜(seaborgium)上也发现了类似的效应。
f-d之争
Nature这 篇论文的作者认为,他们的研究确认了铹元素应该属于f区中的锕系:“如此低的电离势完美地支持了这一想法,”Matthias Schädel说。在于上周退休之前,他一直领导着JAEA的超重原子研究小组。从20世纪80年代开始,他就投身于证明铹元素与f区元素性质相似的前沿 实验中了。
但美国辛辛那提大学的William Jensen则认为,该实验结果推出的结论恰恰相反:他指出,大多数锕系元素的第一电离能都比它们上方的镧系元素高,但铹的第一电离能却比它上方的镥要低,这与其他的锕系元素都不同,更像是d区元素。在发表于3月21日的《化学基础》(Foundations of Chemistry)杂志中,他详尽阐述了将铹放到d区的理由。而 Sato觉得,他的团队计算出来的第一电离能既不能证明铹应该在f区,也不能证明它在d区。IUPAC无机化学部的主席Jan Reedijk也表示,IUPAC对镥和铹的分区暂时还没有官方的意见。刚刚发表的这篇论文,可能会帮助大家重拾对这个问题的讨论,他也补充说,在今年夏 天举行的国际会议中,IUPAC可能也会把这个问题加入议题之中。
Jensen说,许多在实验室埋头搬砖的化学家甚至都没有意识到这个问题,但这是不对的。身为化学家,关注化学元素周期表是否正确和一致是应该做的事。
- 上一篇 >发行规模大增 2022年绿色债券市场扩容可期2022-02-17
- < 下一篇将二氧化碳转化为绿色能源电池2016-03-07





